Arviointimenettely liitteen I muutoksen seurauksena
Arviointimenettely liitteen I muutoksen seurauksena
Arviointimenettely alkaa, kun arvioiva toimivaltainen viranomainen katsoo biosidivalmisteasetuksen liitteen I muutosta koskevan hakemuksen päteväksi. Arvioivalla toimivaltaisella viranomaisella on ryhmää 1, 2, 3, 4 ja 5 koskevissa hakemuksissa 180 päivää ja ryhmää 6 koskevissa hakemuksissa 365 päivää aikaa arvioida hakemusta ja esittää päätelmänsä kemikaalivirastolle.
Arviointimenettelyn aikana hakijaa voidaan pyytää toimittamaan lisätietoja, jos arvioiva toimivaltainen viranomainen pitää niitä tarpeellisina. Hakijan on toimitettava pyydetyt tiedot 180 päivän kuluessa, ellei määräajan lykkääminen ole perusteltua pyydettyjen tietojen luonteen tai poikkeuksellisten olosuhteiden takia.
Jos hakemus, joka koskee tehoaineen lisäämistä biosidivalmisteasetuksen liitteen I ryhmään 1, 2, 3, 4 tai 5, vastaa lisätietoja koskevan pyynnön jälkeen täysin tietopaketin sisältävää aineistoa, joka mahdollistaa käyttötarkoituksen täydellisen riskinarvioinnin, hakija voi pyytää lisäämistä liitteen I ryhmään 6 ja aineiston arviointia sen mukaan.
Vaiheet
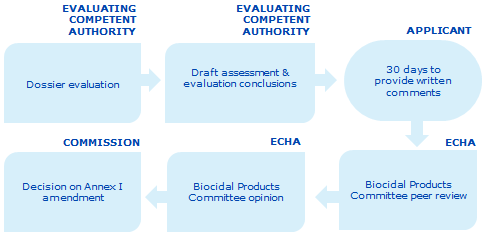
Arviointimenettelyssä on seuraavat vaiheet:
Arvioiva toimivaltainen viranomainen arvioi aineiston.
Arvioiva toimivaltainen viranomainen laatii alustavan arviointikertomuksen ja päätelmät arvioinnistaan.

Alustava arviointikertomus lähetetään hakijalle R4BP 3 -sovelluksen kautta. Hakijalla on 30 päivää aikaa esittää kirjallisia huomautuksia. Arvioiva toimivaltainen viranomainen ottaa kyseiset huomautukset asianmukaisesti huomioon viimeistellessään arviointinsa.

Arviointikertomus lähetetään R4BP 3 -sovelluksen kautta kemikaalivirastolle vertaisarviointiin biosidivalmistekomiteassa.

Biosidivalmistekomitealla on ryhmän 1, 2, 3, 4 ja 5 hakemuksen tapauksessa 180 päivää ja ryhmän 6 hakemuksen tapauksessa 270 päivää aikaa esittää lausuntonsa vertaisarvioinnin muodossa ja toimittaa kyseinen lausunto komissiolle.

Komissio tekee päätöksen hakijan pyynnöstä muuttaa biosidivalmisteasetuksen liitettä I .
Toimijat
Arviointimenettelyn päätoimijat ovat seuraavat:
Hakijat
Hakijoilla on vastuu kaikkien tarvittavien tietojen toimittamisesta aineistoissaan. Niiden on otettava menettelyn eri määräajat huomioon. Hakijat voivat kommentoida aineistoaan koskevaa alustavaa kertomusta menettelyn aikana.
Kemikaalivirasto
Kemikaalivirasto koordinoi lisäämismenettelyä ja tarjoaa hakijoille tarvittavat välineet ja tuen. Kemikaalivirasto vastaa myös biosidivalmistekomitean sihteeristöstä.
Biosidivalmistekomitea
Biosidivalmistekomitea antaa tieteellisiä lausuntoja tehoaineista (hyväksyntä, uusiminen, arviointi ja lisääminen liitteeseen I), unionin lupia biosidituotteille ja vastavuoroisia tunnustuksia. Komitea käsittelee myös tieteellisiä ja teknisiä asioita ja muita kysymyksiä Euroopan komission ja jäsenvaltioiden pyynnöstä. EU:n ja ETA:n jäsenvaltiot nimittävät komitean jäsenet näiden kokemuksen perusteella.
Arvioiva toimivaltainen viranomainen
Arvioiva toimivaltainen viranomainen vastaa hakemusten arvioinnista. Hakija valitsee arvioivan toimivaltaisen viranomaisen.
Euroopan komissio
Jos on näyttöä siitä, että tehoaine ei aiheuta huolta biosidivalmisteasetuksen 28 artiklan 1 kohdassa tarkoitetulla tavalla, Euroopan komissio voi yhdessä biosidivalmisteiden pysyvän komitean kanssa ottaa huomioon biosidivalmistekomitean antaman lausunnon (mukaa luettuina lausunnot nykyisistä ja uusista tehoaineista) ja päättää siitä, muuttaako se biosidivalmisteasetuksen liitettä I vai ei. Komissio toimii puheenjohtajana pysyvässä komiteassa, jossa on edustajia kaikista jäsenvaltioista. Aina kun komissio muuttaa liitettä I, sen on hyväksyttävä erillinen delegoitu säädös jokaisesta aineesta.