Procedura de evaluare pentru modificarea anexei I
Procedura de evaluare pentru modificarea anexei I
Procedura de evaluare începe atunci când o cerere de modificare a anexei I la BPR este considerată valabilă de către autoritatea competentă responsabilă de evaluare. Autoritatea competentă responsabilă de evaluare are la dispoziție 180 de zile în cazul cererilor pentru categoriile 1, 2, 3, 4 și 5 și 365 de zile în cazul cererilor pentru categoria 6 pentru a evalua cererea și a trimite concluziile sale la ECHA.
Pe parcursul procesului de evaluare, solicitantului i se poate cere să ofere informații suplimentare în cazul în care autoritatea competentă responsabilă de evaluare consideră că sunt necesare mai multe date. Solicitantul trebuie să furnizeze informațiile cerute în termen de 180 de zile, cu excepția cazului în care natura datelor solicitate sau apariția unor circumstanțe excepționale justifică o întârziere.
În urma solicitării de informații suplimentare, dacă se constată că o cerere de includere a unei substanțe active în categoria 1, 2, 3, 4 sau 5 din anexa I la BPR respectă pe deplin cerințele unui dosar care conține un pachet de date ce permite evaluarea completă a riscurilor pentru utilizarea prevăzută, solicitantul poate cere ca substanța să fie inclusă în categoria 6 din anexa I, iar dosarul să fie evaluat în consecință.
Etape
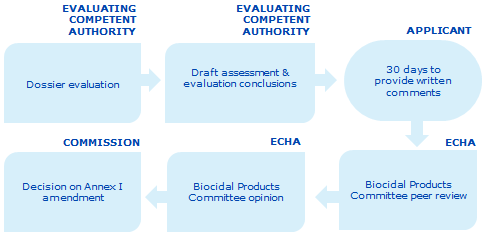
Procedura de evaluare cuprinde următoarele etape:
Autoritatea competentă responsabilă de evaluare realizează evaluarea dosarului.
Autoritatea competentă responsabilă de evaluare întocmește proiectul raportului de evaluare și concluziile evaluării sale.

Proiectul raportului de evaluare este trimis solicitantului prin R4BP 3. Solicitantul are la dispoziție 30 de zile pentru a-și prezenta observațiile în scris. Autoritatea competentă responsabilă de evaluare ia în considerare aceste observații atunci când își finalizează evaluarea.

Raportul de evaluare este transmis la ECHA prin R4BP 3, în vederea evaluării inter pares în cadrul Comitetului pentru produse biocide (CPB)

CPB are la dispoziție 180 de zile în cazul cererilor pentru categoriile 1, 2, 3, 4 și 5 și 270 de zile în cazul cererilor pentru categoria 6 pentru a emite un aviz în urma evaluării inter pares și a transmite acest aviz Comisiei.

Comisia adoptă o decizie cu privire la cererea solicitantului de modificare a anexei I la BPR.
Actori
Principalii actori în procedura de evaluare sunt:
Solicitanții
Solicitanții răspund de furnizarea tuturor informațiilor necesare în dosarele lor. Aceștia trebuie să țină seama de diferitele termene aplicabile pe toată durata procedurii. Pe parcursul procesului, solicitanții au posibilitatea să transmită observații pe marginea proiectului de raport referitor la dosarul lor.
ECHA
ECHA coordonează procedura de includere și le oferă solicitanților instrumentele și sprijinul de care au nevoie. Tot ECHA asigură și activitățile de secretariat pentru Comitetul pentru produse biocide.
Comitetul pentru produse biocide (CPB)
Comitetul pentru produse biocide emite un aviz științific cu privire la substanțele active (aprobare, reînnoire, reexaminare, includere în anexa I), la autorizația Uniunii pentru produse biocide și la recunoașterea reciprocă. De asemenea, comitetul se ocupă de aspectele de natură științifică și tehnică, precum și de alte chestiuni, la cererea Comisiei Europene și a statelor membre. Comitetul este format din membri numiți de statele membre ale UE și de țările SEE, în baza experienței lor.
Autoritățile competente responsabile de evaluare
Autoritatea competentă responsabilă de evaluare are sarcina de a evalua cererile. Autoritatea competentă responsabilă de evaluare este aleasă de solicitant.
Comisia Europeană
Cu condiția să existe dovezi privind faptul că substanța activă nu suscită îngrijorare în sensul articolului 28 alineatul (1) din BPR, Comisia Europeană – împreună cu Comitetul permanent pentru produse biocide – ia în considerare avizul emis de CPB (inclusiv avizele referitoare la substanțele active noi și existente) și hotărăște dacă va modifica sau nu anexa I la BPR. Comitetul permanent este prezidat de Comisie și are în componență reprezentanți din toate statele membre. Ori de câte ori modifică anexa I, Comisia trebuie să adopte un act delegat separat cu privire la fiecare substanță.