Novērtēšanas process I pielikuma grozījumam
Novērtēšanas process I pielikuma grozījumam
Novērtēšanas process sākas brīdī, kad kompetentā iestāde, kas veic novērtēšanu, atzīst pieteikuma par grozījuma izdarīšanu Biocīdu regulas I pielikumā atbilstību. Kompetentās iestādes, kas veic novērtēšanu, rīcībā ir 180 dienas 1., 2., 3., 4. un 5. kategorijas pieteikuma gadījumā un 365 dienas 6. kategorijas pieteikuma gadījumā, lai novērtētu pieteikumu un nosūtītu ECHA savu secinājumu.
Novērtēšanas procesa laikā pieteikuma iesniedzējam var pieprasīt sniegt papildu informāciju, ja kompetentā iestāde, kas veic novērtēšanu, uzskata, ka ir vajadzīga plašāka informācija. Pieteikuma iesniedzējam ir jāiesniedz pieprasītā informācija 180 dienu laikā, ja vien kavējumu neattaisno pieprasīto datu veids vai ārkārtas apstākļi.
Ja pieteikums par aktīvās vielas iekļaušanu Biocīdu regulas I pielikuma 1., 2., 3., 4. vai 5. kategorijā pēc papildu informācijas pieprasījuma ir uzskatāms par pilnībā atbilstošu dokumentāciju ar datu paketi, kas ļauj pienācīgi novērtēt riskus saistībā ar paredzēto lietojumu, pieteikuma iesniedzējs var minēto kategoriju vietā pieprasīt iekļaušanu I pielikuma 6. kategorijā un dokumentācijas attiecīgu novērtēšanu.
Posmi
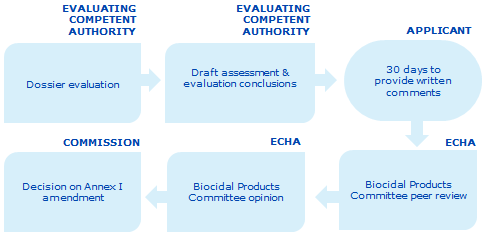
Novērtēšanas procesu veido turpmāk uzskaitītie posmi.
Kompetentā iestāde, kas veic novērtēšanu, novērtē dokumentāciju.
Kompetentā iestāde, kas veic novērtēšanu, sagatavo novērtējuma ziņojuma projektu un sava izvērtējuma secinājumus.

Novērtējuma ziņojuma projektu nosūta pieteikuma iesniedzējam ar R4BP 3 starpniecību. Pieteikuma iesniedzēja rīcībā ir 30 dienas, lai iesniegtu rakstiskus komentārus. Kompetentā iestāde, kas veic novērtēšanu, pienācīgi ņem vērā šos komentārus, pabeidzot sava izvērtējuma izstrādi.

Novērtējuma ziņojumu ar R4BP 3 starpniecību nosūta ECHA salīdzinošai izvērtēšanai Biocīdu komitejā (BK).

BK rīcībā ir 180 dienas 1., 2., 3., 4. un 5. kategorijas pieteikuma gadījumā un 270 dienas 6. kategorijas pieteikuma gadījumā, lai sniegtu atzinumu ar salīdzinošās izvērtēšanas novērtējumu un lai šo atzinumu iesniegtu Komisijai.

Komisija pieņem lēmumu par pieteikuma iesniedzēja pieprasījumu grozīt Biocīdu regulas I pielikumu.
Dalībnieki
Galvenie novērtēšanas procesa dalībnieki ir:
Pieteikuma iesniedzēji
Pieteikumu iesniedzēji ir atbildīgi par visas nepieciešamās informācijas nodrošināšanu savā dokumentācijā. Visa procesa laikā viņiem ir jāpievērš uzmanība dažādiem termiņiem. Pieteikumu iesniedzējiem procesa gaitā ir iespēja sniegt komentārus attiecībā uz novērtējuma ziņojuma projektu par viņu dokumentāciju.
ECHA
ECHA koordinē iekļaušanas procesu un nodrošina pieteikumu iesniedzējiem vajadzīgos rīkus un atbalstu. ECHA arī nodrošina Biocīdu komitejas sekretariātu.
Biocīdu komiteja (BK)
Biocīdu komiteja sniedz zinātnisko atzinumu par aktīvajām vielām (apstiprināšanu, atjaunošanu, pārskatīšanu, iekļaušanu I pielikumā), izsniedz Savienības atļauju biocīdiem un nodrošina savstarpējo atzīšanu. Komiteja arī risina zinātniskos, tehniskos un citus jautājumus pēc Eiropas Komisijas un dalībvalstu pieprasījuma. Komitejā ir ES dalībvalstu un EEZ valstu ieceltie dalībnieki, pamatojoties uz šo personu pieredzi.
Kompetentās iestādes, kas veic novērtēšanu
Kompetentā iestāde, kas veic novērtēšanu, ir atbildīga par pieteikumu izvērtēšanu. Kompetento iestādi, kas veic novērtēšanu, izvēlas pieteikuma iesniedzējs.
Eiropas Komisija
Ja ir pierādījumi, ka aktīvā viela nerada pamatu bažām Biocīdu regulas 28. panta 1. punkta nozīmē, Eiropas Komisija kopā ar Biocīdu pastāvīgo komiteju ņem vērā BK sniegto atzinumu (tostarp, atzinumus par esošām un jaunām aktīvajām vielām) un pieņem lēmumu par to, vai grozīt Biocīdu regulas I pielikumu. Pastāvīgo komiteju vada Komisija, un tajā ir visu dalībvalstu pārstāvji. Vienmēr, kad Komisija groza I pielikumu, tai ir jāpieņem atsevišķs deleģētais akts par katru vielu.